단계적 일상회복(위드코로나)이 시작됨에 따라 코로나19 치료제에 대한 관심이 집중되고 있다. 매경헬스는 국내 제약사로서 코로나19 치료제 정식허가를 획득한 셀트리온의 항체치료제 렉키로나를 시작으로 전 세계 코로나19 치료제의 작용기전과 효과, 부작용을 톺아보려 한다.
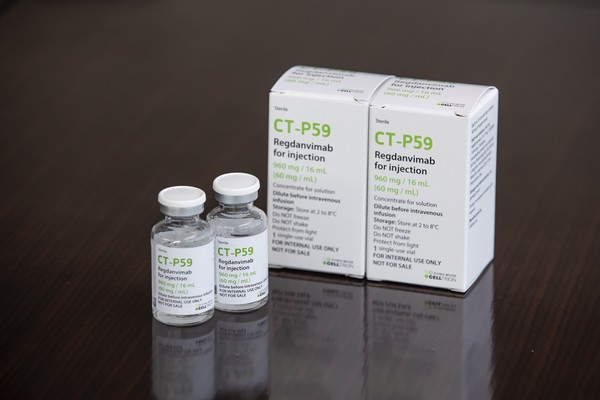
셀트리온의 코로나19 항체치료제 렉키로나는 지난 2월 5일 식품의약품안전처로부터 품목허가를 받았다. 정식 명칭은 ‘렉키로나주960mg(레그단비맙)(단클론항체/유전자재조합)’.
렉키로나주960mg은 코로나19 바이러스의 스파이크 단백질을 표적으로 하는 인간 단클론항체 의약품으로, 중국 햄스터 난소 세포주(Chinese Hamster Ovary cell line)에서 DNA 재조합 기술을 통해 개발됐다.
렉키로나주960mg의 주된 기전은 해당 인간 단클론항체(레그단비맙/Regdanvimab)가 코로나19 바이러스 스파이크 단백질의 수용체 결합 도메인(Receptor Binding Domain)에 결합하여 사람 안지오텐신 전환 효소 2(ACE2) 수용체와의 결합을 차단함으로써, 코로나19를 유발하는 코로나19 바이러스(SARS-CoV-2)의 감염을 억제하는 형태다.
렉키로나주의 적응증은 PCR 검사 등을 통해 코로나19가 확진된 성인으로서, 다음 기준에 모두 해당하는 고위험군 경증 혹은 모든 중등증 환자의 치료라 할 수 있다.
구체적으로 실내 공기에서 산소포화도가 94%를 초과하는 자, 보조적인 산소 공급이 필요하지 않은 자, 투여 전 7일 이내에 증상이 발현한 자 등이다. 또 고위험군 경증은 고령자(50세 초과), 비만(체질량지수[BMI] 30kg/m2 초과), 심혈관질환(고혈압 포함), 만성 폐질환(천식 포함), 당뇨, 만성 신장질환(투석 포함), 만성 간질환, 질환 또는 치료에 의한 면역 억제 상태 등에서 하나 이상에 해당하는 경증 환자라 명시됐다.
특히 면역 억제 상태는 암치료, 골수 또는 장기 이식, 면역결핍, HIV, 겸상 적혈구 빈혈, 지중해 빈혈, 그리고 면역 약화 약물의 장기간 복용 중인 상태 등을 뜻한다.
허가사항 상의 용법 및 용량은 40mg/kg을 60분(±15분)간 정맥으로 단회 점적주입이며, 구체적인 용량 해설 공식은 다음과 같다.
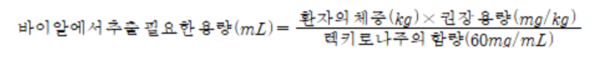
렉키로나주960mg의 사용상의 주의사항에는 ‘이전에 보고되지 않은 예상하지 못한 중대한 이상반응이 발생할 수 있으므로 이 약을 투여 받는 환자에 대한 임상적, 실험실적 모니터링을 주의 깊게 실시 해야한다’는 내용의 경고사항이 포함됐다.
이와 함께 주입관련 반응, 아나필락시스와 같은 과민 반응이 나타날 수 있으므로 환자의 상태를 주의 깊게 모니터링하고, 이러한 증상이나 징후가 관찰될 경우에는 이 약을 즉시 중단하고 적절한 처치를 실시 해야한다는 것이 식약처 등의 공식적인 입장이다.
투여가 제한되는 환자는 렉키로나주 구성 성분(유효성분 : 레그단비맙 / 첨가제 : 폴리소르베이트80, L-히스티딘염산염일수화물, L-히스티딘, L-아르기닌염산염, 주사용수)에 과민성hypersensitivity)이 있는 경우로, 특히 L-아르기닌염산염에 대한 주의가 필요하다.
또 신중한 투여가 필요한 환자는 간장애 및 신장애 환자 등이다.
렉키로나주960mg에 대한 약물 상호작용 시험은 수행되지 않았다. 때문에 레그단비맙의 대사 경로는 규명되지 않았으나, 학술적으로 단클론항체라는 점에서 레그단비맙은 이화 반응경로를 통해 작은 펩티드와 아미노산으로 분해될 것으로 예상된다.
그렇기에 레그단비맙은 신장을 통해 배출되거나 사이토크롬 P450 효소에 의해 대사 되지 않는다. 따라서 신장을 통해 배출되거나 사이토크롬 P450 효소의 기질, 유도체 또는 억제제인 병용약물과의 상호작용 가능성이 낮다는 것이 관련 전문가들의 견해다.
렉키로나주의 임상 단계에서 18명의 경증 코로나19 환자들을 대상으로 이 약 20mg/kg, 40mg/kg, 80mg/kg 또는 위약을 단회 정맥 투여하는 1상 임상시험에서 위약 대비 이 약의 전반적인 안전성 및 유효성을 평가했을 때, 일차 평가변수 상 시험 대상자의 14일까지 연관이 있는 중대한 이상 사례나 주입 관련 반응은 나타나지 않은 것으로 알려졌다.
매경헬스에 여러분의 이야기를 들려주세요.
억울한 혹은 따뜻한 사연을 24시간 기다립니다.
이메일 jebo@mkhealth.co.kr 대표전화 02-2000-5802 홈페이지 기사제보